| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
CYP3A4 (EC50 = 0.25 μM); EGFR
|
|---|---|
| 体外研究 (In Vitro) |
甲磺酸伏美替尼可以抑制 T790M 获得性耐药突变和 EGFR 活性突变[1]。
本研究采用CRISPR方法构建4株EGFR S768I突变细胞系,检测EGFR对阿蒙尼替尼和阿氟替尼的敏感性,阳性对照为第1代(吉非替尼)、第2代(阿法替尼)、第3代(奥西替尼)药物。 结果:本研究结果表明,almonertinib和alflutinib可通过ERK或AKT通路,通过阻断细胞周期和抑制细胞凋亡,以时间依赖性的方式有效抑制罕见EGFR S768I突变的细胞活力和增殖。 结论:这些发现提示,阿莫那替尼和阿氟替尼可能是EGFR S768I突变的非小细胞肺癌患者的潜在治疗选择。[2] |
| 体内研究 (In Vivo) |
从2016年12月27日至2017年8月21日,共有17名患者在4个队列中接受了至少一剂AST2818/alflutinib (20mg、40mg、80mg和160mg QD)。最大耐受剂量尚未达到。最常见的治疗相关ae是1级蛋白尿(25%,3/12)。其他ae包括疲劳、Q-T间隔延长等,均小于10%,为1级或2级。前12例患者的ORR为58.3%(7/12),疾病控制率为91.7%(11/12)。在20mg组中已经观察到深刻和持续的肿瘤消退。以Cmax和AUC 0-24h测量的AST2818血浆暴露呈剂量正比增加。
结论
在第一代EGFR- tkis治疗失败后,AST2818在EGFR T790M突变型NSCLC中耐受性良好,具有良好的临床活性和持久的疾病控制。[1]
|
| 酶活实验 |
阿氟替尼在HLMs中的代谢[3]
在开始实验之前,将HLMs在冰上轻轻解冻。然后,将3µM阿氟替尼(0.5 mg蛋白/mL)加入到100 mM磷酸盐缓冲盐水(PBS;pH 7.4)至总容积为100 μL。37℃孵育3min后,加入1.0 mM NADPH启动反应。孵育1小时后,用相同体积的冰凉乙腈混合终止反应。所有孵育重复进行,然后用UPLC-UV/Q-TOF质谱分析[3] 特异性CYP抑制剂对HLMs的影响[3] 采用HLMs研究CYP酶抑制剂对阿氟替尼代谢的影响。孵育混合物(100µL)由阿氟替尼(3µM)、HLMs (0.5 mg蛋白/mL)、NADPH (1 mM)、PBS (100 mM, pH 7.4)和选择性CYP抑制剂组成。化学抑制剂分别为:CYP1A/ 2c α-萘黄酮(2µM)、CYP2C8槲皮素(20µM)、CYP2C9磺胺苯唑(6µM)、CYP2B6/2C19噻氯匹定(24µM)、CYP2D6奎尼丁(8µM)、CYP2E1氯甲基唑(24µM)、CYP3A酮康唑(2µM)、ABT(1µM)。在加入底物之前,将这些抑制剂与HLMs在NADPH存在下预孵育10分钟。然后,在37°C下孵育60分钟开始反应。最后,加入100µL冰凉的乙腈终止反应。所有的孵育重复进行,在没有或存在抑制剂的情况下评估代谢物的形成[3] 。 重组人CYP同工酶对阿氟替尼的代谢作用[3] 为了鉴定参与阿氟替尼代谢的特异性异构体,将3µM阿氟替尼与重组人CYP1A2、2A6、2B6、2C8、2C9、2C19、2D6、2E1、3A4或3A5 (25 pmol P450/mL)混合,总体积为100 μL。分别加入1 mM NADPH和100µL冰凉乙腈开始和终止反应。37℃孵育60 min。[3] 阿氟替尼对人主要CYP酶的抑制作用[3] 所有cypp异构体特异性探针,如非那西丁、安非他酮、紫杉醇、甲磺丁酰胺、s -甲苯妥英和右美沙芬(分别用于CYP1A2、2B6、2C8、2C9、2C19和2D6)以及咪达唑仑和睾酮(用于CYP3A4),均溶解于甲醇中。阿氟替尼作为100mm的原液溶解在DMSO中。总体积为100 μL,培养基为100 mM PBS,含有混合HLMs (0.5 mg/mL)、探针底物、NADPH (1 mM)和不同浓度的阿氟替尼(0、0.1、0.33、1、3.30、10、33.3和100 μM)。37℃预孵育5 min。在实验条件下,酶浓度与反应体系孵育时间均在线性范围内(补充表S1)。[3] 阿氟替尼和AST5902对人CYP3A4酶的酶促作用[3] 为了评估酶的诱导作用,将7 × 105个肝细胞/mL接种于胶原包被的24孔板中,置于37℃加5% CO2的加湿培养箱中24 h。用人CYP3A4酶诱导剂利福平(10 μM)、阿氟替尼或AST5902(0.003、0.01、0.03、0.1、0.3、1、3或5 μM)或0.1% DMSO(对照组)处理肝细胞,每天1次,连续3天。处理后,按照制造商的方案用TRIzol进行RNA提取。采用PrimeScript RT试剂盒进行cDNA合成。采用SYBR green Premix Ex Taq试剂盒,在StepOnePlus实时PCR系统上进行实时PCR。CYP3A4的正向引物为5 ' -ATCACTAGCACATCATTTGGAG-3 ',反向引物为5 ' -GGAATGGAAAGGTTATTGAGAG-3 '。GAPDH正向引物为5′-AGAAGGCTGGGGCTCATTTG-3′,反向引物为5′-GAGGGGCCATCCACAGTCTTC-3′。以GAPDH为内标,采用比较阈值循环法定量cDNA水平。 |
| 细胞实验 |
细胞存活与生长试验[2]
采用MTT法测定H3255、H3255Cas9+S768I、H3255L858R+S768I、PC9、PC9Cas9+S768I、PC919Del+S768I细胞的活力,以确定不同TKIs的影响。将细胞消化成单细胞悬液,接种于96孔板,在RPMI 1640培养基中培养,每孔5000个细胞/100 μL。去除原始培养基后,每孔加入100μL不同的TKIs处理细胞。细胞培养24或48 h后,每孔中加入20 μL MTT, 37℃孵育4 h,丢弃上清,每孔中加入100 μL DMSO溶液。将96孔板在37℃避光条件下孵育15 min,之后使用微孔板仪在490 nm处测量光密度(OD)。[2] 菌落形成试验[2] 将H3255、H3255Cas9+S768I、H3255L858R+S768I、PC9、PC9Cas9+S768I、PC919Del+S768I细胞接种于6孔板中,密度为每孔500个细胞,接种于2ml培养基中。18 h后,取出培养基,用不同浓度的TKIs孵育细胞。每2-3天更换一次含药培养基。在37℃下培养14天后,丢弃培养基。每孔用PBS缓冲液洗涤,4%多聚甲醛固定15分钟,室温下用吉姆萨染色20分钟。然后丢弃吉姆萨染色液,每孔用双蒸馏水冲洗三至四次。最后自然风干后计数菌落。[2] 细胞增殖试验[2] 将H3255、H3255Cas9+S768I、H3255L858R+S768I、PC9、PC9Cas9+S768I和PC919Del+S768I细胞以每孔5000个细胞的密度接种于96孔板中。18 h后,更换不同的TKIs培养液,孵育48 h,丢弃培养液,用PBS缓冲液洗涤细胞。随后,每口井依次用4%多聚甲醛、3% BSA PBS和0.3% Triton X-100 PBS进行处理。每次处理后,用PBS缓冲液冲洗细胞三次。然后在每孔中加入50 μL的click反应液,标记增殖细胞。细胞在黑暗中孵育30分钟。去除培养基后,细胞洗涤三次。然后,加入50 μL的Hoechst染色剂标记所有细胞核,细胞在黑暗中孵育10分钟,丢弃培养基后,细胞清洗3次,立即荧光显微镜下拍照。 |
| 动物实验 |
Patients with histologically diagnosed, EGFR T790M mutant stage IV NSCLC were considered eligible, and they should have documented disease progression on EGFR-TKIs. In a 3+3 dose-escalation design, AST2818 was orally administered every day on a 21-day cycle at doses ranging from 20mg to 240 mg (NCT02973763). AST2818 was then explored in a dose-expansion cohort at doses ranging from 40 to 240 mg every day. Plasma samples were collected to evaluate pharmacokinetics of AST2818. EGFR T790M mutation in tissue samples was detected by amplification refractory mutation system. The primary endpoint was to determine dose limiting toxicity and objective response rate (ORR). Adverse events (AEs) were evaluated by CTCAE 4.03, and efficacy was assessed per RECIST v1.1 every 6 weeks.[1]
|
| 参考文献 |
[2]. Almonertinib and alflutinib show novel inhibition on rare EGFR S768I mutant cells. Clin Transl Oncol . 2024 May 30. doi: 10.1007/s12094-024-03494-5.
[3]. Alflutinib (AST2818), primarily metabolized by CYP3A4, is a potent CYP3A4 inducer. Acta Pharmacol Sin. 2020 Oct;41(10):1366-1376. |
| 其他信息 |
Alflutinib Mesylate is the mesylate salt form of alflutinib, an orally available selective inhibitor of the epidermal growth factor receptor (EGFR) mutant form T790M, with potential antineoplastic activity. Upon administration, alflutinib specifically binds to and inhibits the tyrosine kinase activity of EGFR T790M, a secondarily acquired resistance mutation. This prevents EGFR T790M-mediated signaling and leads to cell death in EGFR T790M-expressing tumor cells. EGFR, a receptor tyrosine kinase that is mutated in many tumor cell types, plays a key role in tumor cell proliferation and tumor vascularization. Compared to some other EGFR inhibitors, alflutinib may have therapeutic benefits in tumors with T790M-mediated drug resistance.
|
| 分子式 |
C29H35F3N8O5S
|
|---|---|
| 分子量 |
664.699014902115
|
| 精确质量 |
664.24
|
| 元素分析 |
C, 52.40; H, 5.31; F, 8.57; N, 16.86; O, 12.03; S, 4.82
|
| CAS号 |
2130958-55-1
|
| 相关CAS号 |
Firmonertinib;1869057-83-9
|
| PubChem CID |
134828257
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| LogP |
4.4
|
| tPSA |
163Ų
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
14
|
| 可旋转键数目(RBC) |
11
|
| 重原子数目 |
46
|
| 分子复杂度/Complexity |
957
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
WDPGHXINXNBHAS-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C28H31F3N8O2.CH4O3S/c1-6-24(40)33-21-15-22(26(41-17-28(29,30)31)36-25(21)38(4)14-13-37(2)3)35-27-32-12-11-20(34-27)19-16-39(5)23-10-8-7-9-18(19)23;1-5(2,3)4/h6-12,15-16H,1,13-14,17H2,2-5H3,(H,33,40)(H,32,34,35);1H3,(H,2,3,4)
|
| 化学名 |
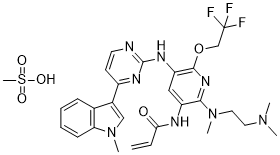
N-[2-[2-(dimethylamino)ethyl-methylamino]-5-[[4-(1-methylindol-3-yl)pyrimidin-2-yl]amino]-6-(2,2,2-trifluoroethoxy)pyridin-3-yl]prop-2-enamide;methanesulfonic acid
|
| 别名 |
Furmonertinib; AST-2818; AST 2818 mesylate; Alflutinib mesylate; Alflutinib (mesylate); AST-2818 mesylate; Firmonertinib mesylate; N-(2-((2-(Dimethylamino)ethyl)(methyl)amino)-5-((4-(1-methyl-1H-indol-3-yl)pyrimidin-2-yl)amino)-6-(2,2,2-trifluoroethoxy)pyridin-3-yl)acrylamide methanesulfonate; Q09ZKD19V0; AST2818 mesylate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 该产品在溶液状态不稳定,请现配现用。 (2). 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 5~20 mg/mL (7.5~30.1 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 0.5 mg/mL (0.75 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 5.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 0.5 mg/mL (0.75 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 5.0 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 0.5 mg/mL (0.75 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5044 mL | 7.5222 mL | 15.0444 mL | |
| 5 mM | 0.3009 mL | 1.5044 mL | 3.0089 mL | |
| 10 mM | 0.1504 mL | 0.7522 mL | 1.5044 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04858958 | Recruiting | Drug: Furmonertinib 160mg Drug: Furmonertinib 240mg |
NSCLC | Allist Pharmaceuticals, Inc. | August 10, 2020 | Phase 1 |
| NCT05987826 | Not yet recruiting | Drug: Furmonertinib | Non-Small Cell Lung Cancer | Shanghai Zhongshan Hospital | August 2023 | Phase 2 |
| NCT04965831 | Not yet recruiting | Drug: Furmonertinib | Lung Adenocarcinoma | Tianjin Medical University Cancer Institute and Hospital |
August 1, 2021 | Phase 2 |
| NCT05466149 | Recruiting | Drug: Furmonertinib | NSCLC | Allist Pharmaceuticals, Inc. | September 27, 2022 | Phase 2 |
| NCT05334277 | Recruiting | Drug: Furmonertinib/Pemetrexed /Carboplatin Drug: Furmonertinib |
Non-small Cell Lung Cancer | Sun Yat-sen University | May 6, 2022 | Phase 2 |