| 规格 | 价格 | |
|---|---|---|
| 500mg | ||
| 1g | ||
| Other Sizes |
| 靶点 |
P-gp (Kd = 5.1 nM)[1]
|
||
|---|---|---|---|
| 体外研究 (In Vitro) |
体外活性:Tariquidar 显示出与 P-gp 的高亲和力结合,Bmax 为 275 pmol/mg。 Tariquidar 显示与 P-gp 底物长春碱和紫杉醇的非竞争性相互作用。 Tariquidar将这些细胞毒素在CHr /supB30细胞中的稳态积累增加至在不表达P-gp的AuxB1细胞中观察到的水平,EC50为487nM。 Tariquidar 能够抑制 P-gp 的钒酸盐敏感 ATP 酶活性 60-70%,有效 IC50 值为 43 NM。 Tariquidar 在较高浓度下可能会抑制其他耐药机制。 1 μM Tariquidar 在体外消除 ABCG2 (BCRP) 介导的喜树碱耐药性。 Tariquidar 增强多种药物的细胞毒性,包括多柔比星、紫杉醇、依托泊苷和长春新碱;在 25-80 nM Tariquidar 存在下可完全逆转耐药性。在 MC26(一种具有内在化学抗性的小鼠结肠癌细胞系)中,阿霉素 IC50 在 0.1 μM Tariquidar 存在下降低五倍(36 vs 7 nM)。在获得性化疗耐药的小鼠乳腺癌、人小细胞肺癌和人卵巢癌细胞系(EMT6/AR1.0、H69/LX4和2780 AD)中,体外阿霉素IC50比对照组低22-150倍。存在 0.1 μM Tariquidar。从培养系统中除去 Tariquidar 后,P-gp 抑制持续 23 小时。 Tariquidar 在美国国家癌症研究所 (NCI)/ADRRES 源自 MCF7WT 乳腺癌细胞系的多细胞肿瘤球体模型中恢复了阿霉素和长春碱的细胞毒性。
酶活性测定:AuxB1 和 CHrB30 细胞在 12 孔(24 mm)组织培养皿中生长至汇合,并测量 [3H]-长春花碱的稳态积累。通过添加 0.1 μ Ci [3H]-长春花碱和未标记的长春碱至终浓度 100 nM 来启动积累。 [3H]-紫杉醇的积累使用0.1μCi[3H]-紫杉醇和未标记的药物至1μM的终浓度来测量。将细胞在 1 mL 反应体积中于 37 ℃、5% CO2 下孵育 60 分钟,以达到稳态。在 10-9 - 10-6 M 浓度范围内研究调节剂 XR9576 对 [3H]-配体积累的影响。调节剂从 DMSO 库存中添加,最终溶剂浓度为 0.2% (v/v)。细胞收获后,通过液体闪烁计数测量累积的药物并标准化细胞蛋白质含量。累积量作为调节剂浓度的函数的图与一般剂量反应方程拟合: Y={(ab)/(1+(X/c)d)}+b 其中: Y=反应; a=初始响应; b=最终响应; c=EC50浓度; d=斜率值; X=药物浓度。细胞测定:将细胞以 800 个/孔接种到 96 孔板中,加入 100 μL 培养基,并在 37 ℃ 下孵育 4 小时。随后添加不同浓度的调节剂或溶剂对照(50 μL/孔),并在添加细胞毒性药物之前再孵育 1 小时。添加细胞毒性药物 (50 μL),以在四孔中得到一定范围的最终浓度。再孵育 4 天后,使用磺基罗丹明 B 测定法评估贴壁细胞的细胞增殖。 |
||
| 体内研究 (In Vivo) |
发现 Tariquidar(2-8 mg/kg,口服)可显着增强多柔比星(5 mg/kg,静脉注射)体内对 MC26 小鼠结肠癌的抗肿瘤活性。在人类肿瘤异种移植物中,在裸鼠中联合给予 XR9576(6 -12 mg/kg po)可完全恢复紫杉醇、依托泊苷和长春新碱对两种高度耐药的 MDR 人类肿瘤异种移植物(2780AD、H69/LX4)的抗肿瘤活性。
|
||
| 酶活实验 |
P-gp在CHrB30膜中的ATP水解活性[1]
先前描述的比色测定法用于测量ATP水解后无机磷酸盐的释放(Chifflet等人,1988)。膜(1 μg蛋白)与Na2ATP(2 mm),总测定体积为50 μl缓冲液,含(mm):Tris pH 7.4 50,MgSO4 5,0.02%NaN3,NH4Cl 150用于20 最低37°C。ATP酶活性与40呈线性关系 最低37°C。调节剂(来自二甲基亚砜库存)和ATP酶抑制剂钒酸盐的添加浓度范围为10−9–10–5 m.最终DMSO浓度总是<1%,已知该水平不会改变ATP酶活性。药物对ATP酶活性的影响符合一般的剂量-反应关系(见上文) 特异性药物与P-糖蛋白结合[1] 如前所述,使用快速过滤测定法测量[3H]-长春碱、[3H]-紫杉醇和[3H]-XR9576与CHrB30膜中P-gp的结合(Ferry等人,1992)。将膜与适当的放射性配体在总缓冲液体积为200的条件下孵育 μl(50 mm Tris pH 7.4),为期2-3年 h以达到平衡。洗涤缓冲液(3 ml)含有20 mm MgSO4,20 mm Tris(pH 7.4),并且样品在真空下通过过滤歧管中的单个GF/F过滤器过滤以分离结合的和游离的配体。进一步洗涤后(2×3 ml)通过液体闪烁计数测定结合配体的量。非特异性结合被定义为在存在至少100倍过量的竞争配体的情况下结合的[3H]-配体的量(如结果所示),并从所有值中减去。 [3H]-配体结合的容量和亲和力的测定是通过饱和等温线分析实现的。将膜与增加浓度的标记药物和结合量(pmol mg−1)绘制为自由配体浓度的函数。 |
||
| 细胞实验 |
细胞培养[1]
中国仓鼠卵巢亲代(敏感)AuxB1和抗性CHrB30细胞如前所述在含有10%胎牛血清的α-最低必需培养基(α-MEM)中生长(Kartner等人,1983)。通过在秋水仙碱中逐步选择衍生自AuxB1细胞的CHrB30细胞(Kartner等人,1983)表达P-gp,并且通过在培养基中补充30 μg ml−1秋水仙碱 质膜制备[1] 如前所述(Lever,1977),在使用氮空化和蔗糖密度离心收集破坏CHrB30细胞后制备质膜。最终的膜制剂储存在−70°C,蛋白质浓度为5-10 毫克 ml–1在含有0.25的缓冲液中 m蔗糖,10 mm Tris HCI(pH 7.5),并且包括蛋白酶抑制剂亮蛋白肽(0.1 毫克 ml−1),pepstatin A(0.1 毫克 ml−1)和苯甲脒(1 mm) 稳态药物积累试验[1] AuxB1和CHrB30细胞在12孔(24 mm)组织培养皿,并且如前所述测量[3H]-长春碱的稳态积累(Martin等人,1997)。通过添加0.1开始积累 μCi[3H]-长春碱和未标记的长春碱,最终浓度为100 nm。[3H]-紫杉醇的积累用0.1 μCi[3H]-紫杉醇和未标记药物,最终浓度为1 μm。将细胞在反应体积为1 60毫升 在37°C、5%CO2的条件下,以达到稳态。在10−9–10−6的浓度范围内,研究了调节剂XR9576和GF120918对[3H]-配体积累的影响 m.从DMSO原料中加入调节剂,得到0.2%(v v−1)的最终溶剂浓度。细胞采集后,通过液体闪烁计数测量积聚的药物,并对细胞蛋白质含量进行归一化。累积量作为调节剂浓度的函数的图符合一般的剂量反应方程(De Lean等人,1978) 使用几种浓度的放射性标记药物(1-300 nm)在1的存在和不存在下 μm GF120918,并在60 min周期,如上所述。 |
||
| 动物实验 |
|
||
| 参考文献 | |||
| 其他信息 |
1 The kinetics and nature of equilibrium binding were used to characterize the molecular interaction of the anthranilic acid derivative [3H]-XR9576 with the multidrug resistance P-glycoprotein (P-gp). XR9576 displayed specific high-affinity binding to P-gp (Bmax = 275 pmol mg-1, Kd = 5.1 nM). The transport substrates [3H]-vinblastine and [3H]-paclitaxel displayed 4 fold and 20 fold lower affinity respectively for P-gp. The duration of action of XR9576 with P-gp was increased in comparison to that of vinblastine which displayed a slower rate of association and a faster dissociation rate. 2 The relative affinities of several modulators and transport substrates to interact with P-gp were determined from displacement drug equilibrium binding assays. Vinblastine and paclitaxel could only fractionally displace [3H]-XR9576 binding, displaying Ki values significantly different from their measured Kd values. This suggests a non-competitive interaction between XR9576 and the P-gp substrates vinblastine and paclitaxel. 3 XR9576 was shown to be a potent modulator of P-gp mediated [3H]-vinblastine and [3H]-paclitaxel transport as it increased the steady-state accumulation of these cytotoxics in CHrB30 cells to levels observed in non-P-gp-expressing AuxB1 cells (EC50 = 487+/-50 nM). This inhibition of drug transport is not mediated through competition for transport since [3H]-XR9576 accumulation was not influenced by P-gp expression or function. 4 These results demonstrate that the P-gp modulator XR9576 exhibits greater selectivity, duration of inhibition and potency of interaction with this transporter than any other reported modulators. Several lines of evidence suggest that XR9576 inhibits P-gp function by binding at a site which is distinct from the site of interaction of transport substrates. The two sites may be classified as serving modulatory or transport functions.[1]
The overexpression of P-glycoprotein (P-gp) on the surface of tumor cells causes multidrug resistance (MDR). This protein acts as an energy-dependent drug efflux pump reducing the intracellular concentration of structurally unrelated drugs. Modulators of P-gp function can restore the sensitivity of MDR cells to such drugs. XR9576 is a novel anthranilic acid derivative developed as a potent and specific inhibitor of P-gp, and in this study we evaluate the in vitro and in vivo modulatory activity of this compound. The in vitro activity of XR9576 was evaluated using a panel of human (H69/LX4, 2780AD) and murine (EMT6 AR1.0, MC26) MDR cell lines. XR9576 potentiated the cytotoxicity of several drugs including doxorubicin, paclitaxel, etoposide, and vincristine; complete reversal of resistance was achieved in the presence of 25-80 nM XR9576. Direct comparative studies with other modulators indicated that XR9576 was one of the most potent modulators described to date. Accumulation and efflux studies with the P-gp substrates, [3H]daunorubicin and rhodamine 123, demonstrated that XR9576 inhibited P-gp-mediated drug efflux. The inhibition of P-gp function was reversible, but the effects persisted for >22 h after removal of the modulator from the incubation medium. This is in contrast to P-gp substrates such as cyclosporin A and verapamil, which lose their activity within 60 min, suggesting that XR9576 is not transported by P-gp. Also, XR9576 was a potent inhibitor of photoaffinity labeling of P-gp by [3H]azidopine implying a direct interaction with the protein. In mice bearing the intrinsically resistant MC26 colon tumors, coadministration of XR9576 potentiated the antitumor activity of doxorubicin without a significant increase in toxicity; maximum potentiation was observed at 2.5-4.0 mg/kg dosed either i.v. or p.o. In addition, coadministration of XR9576 (6-12 mg/kg p.o.) fully restored the antitumor activity of paclitaxel, etoposide, and vincristine against two highly resistant MDR human tumor xenografts (2780AD, H69/LX4) in nude mice. Importantly all of the efficacious combination schedules appeared to be well tolerated. Furthermore, i.v. coadministration of XR9576 did not alter the plasma pharmacokinetics of paclitaxel. These results demonstrate that XR9576 is an extremely potent, selective, and effective modulator with a long duration of action. It exhibits potent i.v. and p.o. activity without apparently enhancing the plasma pharmacokinetics of paclitaxel or the toxicity of coadministered drugs. Hence, XR9576 holds great promise for the treatment of P-gp-mediated MDR cancers.[2] |
| 分子式 |
C40H46N4O12S2
|
|
|---|---|---|
| 分子量 |
838.94
|
|
| 精确质量 |
838.255
|
|
| 元素分析 |
C, 57.27; H, 5.53; N, 6.68; O, 22.88; S, 7.64
|
|
| CAS号 |
625375-84-0
|
|
| 相关CAS号 |
206873-63-4;625375-84-0 (mesylate);1992047-62-7 (2HCl); 625375-83-9 (methanesulfonate hydrate)
|
|
| PubChem CID |
10079227
|
|
| 外观&性状 |
Solid powder
|
|
| LogP |
7.939
|
|
| tPSA |
240.24
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
14
|
|
| 可旋转键数目(RBC) |
11
|
|
| 重原子数目 |
58
|
|
| 分子复杂度/Complexity |
1130
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
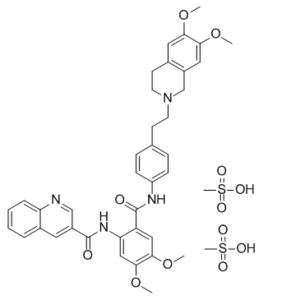
S(C)(=O)(=O)O.S(C)(=O)(=O)O.O(C)C1C(=CC2=C(C=1)CN(CCC1C=CC(=CC=1)NC(C1=CC(=C(C=C1NC(C1=CN=C3C=CC=CC3=C1)=O)OC)OC)=O)CC2)OC
|
|
| InChi Key |
FBCFBFPCZHHRMA-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C38H38N4O6.2CH4O3S/c1-45-33-18-25-14-16-42(23-28(25)19-34(33)46-2)15-13-24-9-11-29(12-10-24)40-38(44)30-20-35(47-3)36(48-4)21-32(30)41-37(43)27-17-26-7-5-6-8-31(26)39-22-27;2*1-5(2,3)4/h5-12,17-22H,13-16,23H2,1-4H3,(H,40,44)(H,41,43);2*1H3,(H,2,3,4)
|
|
| 化学名 |
N-[2-[[4-[2-(6,7-dimethoxy-3,4-dihydro-1H-isoquinolin-2-yl)ethyl]phenyl]carbamoyl]-4,5-dimethoxyphenyl]quinoline-3-carboxamide dimesylate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.1920 mL | 5.9599 mL | 11.9198 mL | |
| 5 mM | 0.2384 mL | 1.1920 mL | 2.3840 mL | |
| 10 mM | 0.1192 mL | 0.5960 mL | 1.1920 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|---|
|
|
|
|---|
|
|