| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
MGL/monoacylglycerol lipase (IC50 = 93 nM)
|
|---|---|
| 体外研究 (In Vitro) |
Pristimerin 已被证明可以抑制纯和未纯化的 MGL(转染的 HeLa 细胞裂解物)的活性,IC50 分别为 93±8 nM 和 398±68 nM。 Pristimerin 是一种快速、可逆、非竞争性的 MGL 抑制剂。通过与调节性半胱氨酸(可能是 Cys208)形成极性接触,prismerin 与 MGL 的结合可能会增强[1]。 Pristimerin 对 HFLS-RA 和 HUVEC 细胞的活力具有剂量和时间依赖性影响。 Pristimerin 降低 VEGF 引起的 VEGFR2 自身磷酸化,并减少 VEGF 产生的 VEGFR2 介导的信号通路的激活 [2]。
|
| 体内研究 (In Vivo) |
Pristimerin抑制肿瘤血管生成和炎症。 Pristimerin 显着降低血清中促血管生成因子(如 TNF-α、Ang-1 和 MMP-9)的表达,并显着降低发炎关节滑膜组织中的血管密度[2]。
类风湿性关节炎(RA)是一种进行性炎症性自身免疫性疾病。随着类风湿性关节炎的进展,滑膜滑膜增生造成缺氧、炎症环境,诱导血管生成。滑膜组织的进一步血管化促进了包膜的生长和炎性白细胞的持续浸润,从而使疾病永久化。pritimerin抑制炎症和肿瘤血管生成。本研究主要探讨普里替木素对佐剂诱导的关节炎大鼠血管生成的抑制作用及其分子机制。研究结果首次清楚地表明,Pristimerin可显著降低炎症关节滑膜组织中的血管密度,并降低血清中促血管生成因子的表达,包括TNF-α、Ang-1和MMP-9。Pristimerin还降低了滑膜中VEGF和p-VEGFR2的表达,而VEGFR2的总量保持不变。pritimerin在体外抑制主动脉环血管的发芽,抑制vegf诱导的HFLS-RA迁移。Pristimerin还抑制了vegf诱导的HUVECs增殖、迁移和成管,阻断了vegf诱导的VEGFR2的自磷酸化,从而下调了vegf诱导的HUVECs中活化的PI3K、AKT、mTOR、ERK1/2、JNK和p38信号通路。研究结果表明,pritimerin在大鼠模型和体外通过中断VEGFR2激活的靶向抑制滑膜血管生成。因此,pritimerin有潜力作为血管生成抑制剂治疗类风湿关节炎。 |
| 酶活实验 |
MGL抑制剂的筛选[1]
光谱收集由2000种化合物组成,在10毫米二甲基亚砜(DMSO)溶液中提供。我们汇集了10个化合物组,并在浓度为1 μM的情况下进行主筛选。阳性组(MGL抑制率≥50%)的单个化合物在10 μM处进行二次筛选。使用新批次的干化合物生成了全浓度-抑制曲线。 酶化验[1] 制备纯化的重组大鼠MGL,并按先前描述的方法测定酶活性(King et al., 2007)。采用TOPO克隆法将大鼠ABHD6或ABHD12全长亚克隆到pEF-V5/His载体上,并进行DNA测序验证。用superect试剂瞬时转染pEF6载体、ABHD6-V5-pEF6或ABHD12-V5-pEF6。转染48小时后,收获细胞,用50 mM Tris-Cl, pH 8.0,含0.32 M蔗糖制备匀浆。ABHD活性采用改进的MGL测定程序(pH 7.5,每次反应3 μg蛋白,37°C下30分钟)测量(King等,2007)。提取样品(King et al., 2007)并通过液相色谱/质谱(LC/MS)进行分析(见下文)。模拟转染的HeLa细胞的2- ag水解酶活性(pmol/min/mg蛋白)为1.4±0.05,转染pef6(仅载体)的细胞为1.3±0.01,转染abhd6的细胞为6.9±0.2 (n = 3)。FAAH和DGL活性在大鼠脑匀浆中测量,如所述。以pCMV-Flag-rNAAA稳定转染HEK293细胞,用superect试剂制备重组NAAA蛋白,用G418 (0.3 mg/ml)筛选。收集细胞,用20 mM Tris-HCl (pH 7.5)和0.32 M蔗糖超声处理,800 × g 4°C离心15 min,上清12000 × g 4°C离心30 min。将颗粒悬浮在磷酸盐缓冲盐水(PBS)中,在-80°C下进行2次冻融循环。将悬浮液在4℃下105000 × g离心1小时,含rNAAA的上清液在-80℃保存至使用。底物(50 μM十六烯乙醇酰胺)与蛋白(10 μg)结合,在37℃条件下,最终体积为0.2 ml的缓冲液(50 mM磷酸氢钠缓冲液,pH 5.0, 0.1% Triton X-100, 3 mM DTT)中测定NAAA活性。加入含有1 nmol十七烷酸的0.2 ml冷甲醇停止反应。MGL、ABHD和NAAA检测采用LC/MS,色谱柱为XDB Eclipse C18 (2.1×30 mm i.d, 1.8 μm,),流速为0.6 ml/min,检测时间为0.6 min,溶剂为95%甲醇和5%水,均含有0.25%乙酸和5mm乙酸铵。柱温为50℃。样品在负电模式下进行电喷雾电离分析。毛细管电压4 kV,破碎器电压100 V,雾化器压力60 psi。干燥气体为N2,流速为13升/分钟,温度为350℃。以十六烷酸为标准(m/z = 269),在选择离子监测(SIM)模式下监测适宜的酶活性产物(MGL和ABHD, m/z = 281, NAAA, m/z = 267)。 |
| 细胞实验 |
将 HFLS-RA(5 × 103 个细胞/mL)或 HUVEC(1 × 104 个细胞/孔)接种于 96 孔板中,并在正常生长培养基中培养 24 小时。然后将细胞与不同浓度的Pristimerin(0、0.125、0.25、0.5 μM)一起孵育。 Pristimerin 对 HUVEC 活力的影响是在 VEGF 诱导的条件下测定的。通过 MTT 测定来量化细胞活力。培养结束前4小时,每孔加入30 μL MTT溶液(5.0 mg/mL)。不含Pristimerin 或VEGF 的细胞作为载体对照[2]。
|
| 动物实验 |
Primary cortical neuron cultures were prepared from embryonic day 18-20 Wistar rats (Stella et al., 2001). Cultures were maintained for 10 days at 37°C with 5% CO2 before treatment with pristimerin (1 μM), euphol (10 μM), NAM (1 μM) or vehicle (0.1% DMSO in Dulbecco's Modified Eagle Medium (DMEM)) for 30 min at 37°C. Reactions were stopped by washing with ice-cold PBS and cells were harvested in 2 ml 50% methanol. Lysates were vortexed for 10 s, protein concentrations were measured by bicinchoninic acid (BCA) protein assay (Pierce, Rockford, IL), and samples were extracted in 4 ml of ice-cold methanol/chloroform/water (1:2:1, vol:vol:vol) containing 0.5 nmol of 2-[2H8]-AG, and 10 pmol each of [2H4]-PEA, added as internal standard. Organic phases were recovered, evaporated under N2, reconstituted in 50 μl chloroform/methanol (1:3, vol:vol) and analyzed by LC/MS as described (Astarita and Piomelli, 2009).[1]
Pristimerin prevents arthritis progression and decreases the severity of arthritis in AA rats[2] To examine the effect of pristimerin on arthritis, the clinical and histopathological characteristics of the SD rat model of Mtb-induced arthritis, which shares immunological and pathological features with human, were examined RA. AA rats were injected daily intraperitoneally with Pristimerin from day 11 to day 24 after initial immunization; the control rats received DMSO (0.4%). The arthritis severity scores and back metatarsal volume of vehicle-treated rats were significantly increased... |
| 毒性/毒理 (Toxicokinetics/TK) |
mouse LD50 oral 8 gm/kg
mouse LD50 intraperitoneal 200 mg/kg mouse LD50 subcutaneous 400 mg/kg |
| 参考文献 | |
| 其他信息 |
Pristimerin is a carboxylic ester.
Pristimerin is a quinone methide triterpenoid researched for its anti-cancer potential. Pristimerin has been reported in Celastrus paniculatus, Celastraceae, and other organisms with data available. |
| 分子式 |
C30H40O4
|
|---|---|
| 分子量 |
464.65
|
| 精确质量 |
464.292
|
| 元素分析 |
C, 77.55; H, 8.68; O, 13.77
|
| CAS号 |
1258-84-0
|
| 相关CAS号 |
Celastrol;34157-83-0
|
| PubChem CID |
159516
|
| 外观&性状 |
Typically exists as Orange to reddish brown solid at room temperature
|
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
607.7±55.0 °C at 760 mmHg
|
| 熔点 |
219.5°C
|
| 闪点 |
195.1±25.0 °C
|
| 蒸汽压 |
0.0±3.9 mmHg at 25°C
|
| 折射率 |
1.582
|
| LogP |
7.54
|
| tPSA |
63.6
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
34
|
| 分子复杂度/Complexity |
1120
|
| 定义原子立体中心数目 |
6
|
| SMILES |
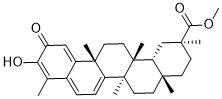
C[C@](C1=CC=C(C(C)=C2O)C3=CC2=O)(CC[C@]4(C)[C@@]5([H])C[C@@](C(OC)=O)(C)CC4)[C@]5(CC[C@]13C)C
|
| InChi Key |
JFACETXYABVHFD-WXPPGMDDSA-N
|
| InChi Code |
InChI=1S/C30H40O4/c1-18-19-8-9-22-28(4,20(19)16-21(31)24(18)32)13-15-30(6)23-17-27(3,25(33)34-7)11-10-26(23,2)12-14-29(22,30)5/h8-9,16,23,32H,10-15,17H2,1-7H3/t23-,26-,27-,28+,29-,30+/m1/s1
|
| 化学名 |
methyl (2R,4aS,6aR,6aS,14aS,14bR)-10-hydroxy-2,4a,6a,6a,9,14a-hexamethyl-11-oxo-1,3,4,5,6,13,14,14b-octahydropicene-2-carboxylate
|
| 别名 |
UNII-28ZK7PR57S; Celastrol-methylether; Celastrol methyl ester; Celastrol-methylether; Pristimerine; GNF-PF-476; CHEBI:8416; MFCD01711331; Pristimerin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMF : 25 mg/mL (~53.81 mM)
DMSO : ~20 mg/mL (~43.04 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (4.30 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1522 mL | 10.7608 mL | 21.5216 mL | |
| 5 mM | 0.4304 mL | 2.1522 mL | 4.3043 mL | |
| 10 mM | 0.2152 mL | 1.0761 mL | 2.1522 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|
|