| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| 5g |
|
||
| Other Sizes |
|

| 体外研究 (In Vitro) |
酮咯酸 (RS37619) 盐(0-30 μM;48 小时)可成功杀死口腔癌细胞[4]。在 H357 细胞中,酮咯酸盐(0–5 μM;48 小时)会导致细胞凋亡并抑制 DDX3 蛋白的产生[4]。酮咯酸盐(0-2.5 μM;0-16 小时)可抑制口腔癌细胞生长[4]。通过直接与 DDX3 相互作用,酮咯酸盐 (0–50 μM) 抑制 ATP 酶活性[4]。
|
|---|---|
| 体内研究 (In Vivo) |
在兔子中,酮咯酸 (RS37619) 或 0.4% 酮咯酸氨丁三醇滴眼液对眼睛表现出有效的抗炎作用[1]。酮咯酸(4 mg/kg/天,口服;2 周)不会对大鼠牙槽窝骨小梁体积分数产生负面影响[2]。在大鼠中,鞘内注射酮咯酸(60 μg)可减轻脊髓缺血引起的损伤[3]。暴露于酮咯酸盐(20 和 30 mg/kg;腹腔注射;每周两次,持续三周)的小鼠口腔癌发生率较低[4]。
|
| 细胞实验 |
细胞活力测定 [4]
细胞类型: HOK、SCC4、SCC9 和 H357 细胞 测试浓度: 0-30 μM 孵育时间:48小时 实验结果:对H357、SCC4和SCC9细胞的IC50分别为2.6、7.1和8.1 μM。而正常的HOK细胞系没有表现出任何细胞死亡效应。 细胞增殖测定[4] 细胞类型: H357 测试浓度: 0.5、1.0、1.5、2.0 和 2.5 μM 孵育时间:0、8和16小时 实验结果:抑制增殖。 蛋白质印迹分析[4] 细胞类型: H357 测试浓度: 1、2.5 和 5 μM 孵育时间:48 小时 实验结果:与 DMSO 处理的细胞相比,DDX3 蛋白表达水平显着降低,但并未完全消除。上调E-钙粘蛋白的表达。 细胞凋亡分析[4] 细胞类型: H357 测试浓度: 2.5 和 5 μM 孵育时间:48小时 实验结果:诱导细胞凋亡。 |
| 动物实验 |
Animal/Disease Models: New Zealand White rabbits (2.0–2.7 kg), LPS endotoxin-induced ocular inflammation[1]
Doses: 50 μL ketorolac tromethamine ophthalmic solution 0.4% Route of Administration: In eyes, twice, 2 hrs (hours) and 1 hour before LPS challenge Experimental Results: Resulted in a nearly complete inhibition (98.7%) of LPS endotoxin-induced increases in FITC (fluorescein isothiocyanate)-dextran in the anterior chamber, and resulted in a nearly complete inhibition (97.5%) of LPS endotoxin-induced increases in aqueous PGE2 concentrations in the aqueous humor. Animal/Disease Models: Male Wistar rats (400–450 g), spinal cord ischemia model[3] Doses: 30 and 60 μg Route of Administration: Intrathecal injection , 1 h before the ischemia induction for once Experimental Results: Dramatically decreased the motor disturbances and improved the survival rate at 60 μg. Animal/Disease Models: Dramatically decreased the motor disturbances and improved the survival rate at 60 μg. Doses: 20 mg/kg and 30 mg/kg Route of Administration: IP injection, two times in a week for 3 weeks |
| 参考文献 |
[1]. Waterbury LD, et al. Comparison of cyclooxygenase inhibitory activity and ocular anti-inflammatory effects of ketorolac tromethamine and bromfenac sodium. Curr Med Res Opin. 2006 Jun;22(6):1133-40.
[2]. Fracon RN, et al. Treatment with paracetamol, ketorolac or etoricoxib did not hinder alveolar bone healing: a histometric study in rats. J Appl Oral Sci. 2010 Dec;18(6):630-4. [3]. Hsieh YC, et al. Intrathecal ketorolac pretreatment reduced spinal cord ischemic injury in rats. Anesth Analg. 2005 Apr;100(4):1134-9. [4]. Samal SK, et al. Ketorolac salt is a newly discovered DDX3 inhibitor to treat oral cancer. Sci Rep. 2015 Apr 28;5:9982. |
| 分子式 |
C15H13N1O3
|
|
|---|---|---|
| 分子量 |
255.27
|
|
| 精确质量 |
255.089
|
|
| CAS号 |
74103-06-3
|
|
| 相关CAS号 |
Ketorolac tromethamine salt;74103-07-4;(S)-Ketorolac;66635-92-5;(R)-Ketorolac;66635-93-6;Ketorolac-d5;1215767-66-0;Ketorolac hemicalcium;167105-81-9;Ketorolac-d4;1216451-53-4
|
|
| 外观&性状 |
Solid powder
|
|
| 密度 |
1.3±0.1 g/cm3
|
|
| 沸点 |
493.2±40.0 °C at 760 mmHg
|
|
| 熔点 |
160-161°C
|
|
| 闪点 |
252.1±27.3 °C
|
|
| 蒸汽压 |
0.0±1.3 mmHg at 25°C
|
|
| 折射率 |
1.659
|
|
| LogP |
2.08
|
|
| tPSA |
59.3
|
|
| InChi Key |
OZWKMVRBQXNZKK-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C15H13NO3/c17-14(10-4-2-1-3-5-10)13-7-6-12-11(15(18)19)8-9-16(12)13/h1-7,11H,8-9H2,(H,18,19)
|
|
| 化学名 |
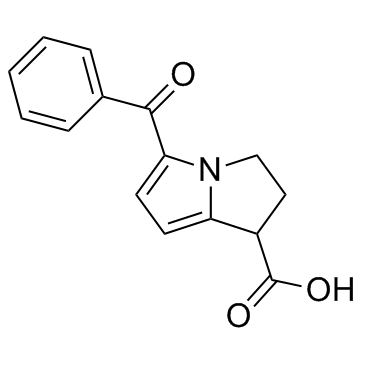
5-benzoyl-2,3-dihydro-1H-pyrrolizine-1-carboxylic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month Note: Please store this product in a sealed and protected environment, avoid exposure to moisture. |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体外实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.9174 mL | 19.5871 mL | 39.1742 mL | |
| 5 mM | 0.7835 mL | 3.9174 mL | 7.8348 mL | |
| 10 mM | 0.3917 mL | 1.9587 mL | 3.9174 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。